




 ,核磁共振氢谱显示只有一组峰,X的结构简式为
,核磁共振氢谱显示只有一组峰,X的结构简式为
 受体拮抗剂,其合成路线如下。
受体拮抗剂,其合成路线如下。



 ),写出相应的化学方程式:
),写出相应的化学方程式: C2H4(g)+H2(g) △H1=+125kJ·mol-1
C2H4(g)+H2(g) △H1=+125kJ·mol-1 C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1
C2H4(g)+CO(g)+H2O(g) △H2=+177kJ·mol-1 2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
2C2H4(g)+2H2O(g) △H3=-211.6kJ·mol-1
 +C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
+C(Ea为活化能,k为速率常数,R和C为常数)。反应的活化能Ea=
 4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比
4CO2(g)+6H2O(g)。在800℃时用乙烷氧气氧化裂解制乙烯,乙烷的转化率、乙烯的选择性和收率随投料比 的变化关系如图所示:
的变化关系如图所示:
 ×100%
×100% =2而不采用选择性更高的
=2而不采用选择性更高的 =3.5,除可防止积碳外,另一原因是
=3.5,除可防止积碳外,另一原因是 <2时,
<2时, 越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是
越小,乙烷的转化率越大,乙烯的选择性和收率越小的原因是 2C2H4(g)+2H2O(g)的Kp=
2C2H4(g)+2H2O(g)的Kp= 氢化制备
氢化制备 。使用不同催化剂,
。使用不同催化剂, 的还原产物不同。
的还原产物不同。



 (g)和5mol
(g)和5mol  (g)仅发生上述反应1和反应2,达到平衡时测得CO为0.2mol,
(g)仅发生上述反应1和反应2,达到平衡时测得CO为0.2mol,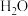 (g)为1mol。
(g)为1mol。 体积分数大于25%
体积分数大于25% 的平衡转化率增大
的平衡转化率增大
 的物质的量分数随温度升高而增大的主要原因是
的物质的量分数随温度升高而增大的主要原因是 的平衡转化率增大,其主要原因是
的平衡转化率增大,其主要原因是 和2mol
和2mol  发生反应:
发生反应:
 ,经过10min达到平衡时体系的压强为原来压强60kPa的
,经过10min达到平衡时体系的压强为原来压强60kPa的 倍。该温度下,反应平衡常数
倍。该温度下,反应平衡常数 ,为
,为 。反应开始到恰好平衡时
。反应开始到恰好平衡时 分压变化速率为
分压变化速率为 。(已知:平衡分压代替平衡浓度计算。分压等于总压×物质的量分数)。
。(已知:平衡分压代替平衡浓度计算。分压等于总压×物质的量分数)。 


 +H2O
+H2O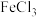 溶液显紫色的结构简式
溶液显紫色的结构简式 和
和 为原料,制备
为原料,制备 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)  是高效光催化剂,可用四氯化钛(
是高效光催化剂,可用四氯化钛( )来制备
)来制备 。
。



 与
与 反应生成
反应生成 、
、 和氧气的热化学方程式为
和氧气的热化学方程式为 ,则E_______(填选项字母)。
,则E_______(填选项字母)。| A.大于a | B.小于a | C.等于a | D.无法确定 |
 和0.2mol
和0.2mol ,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中
,发生反应Ⅰ,经过4min达到平衡状态,平衡时测得容器中 的物质的量为0.02mol。
的物质的量为0.02mol。 的反应速率
的反应速率
 的平衡转化率
的平衡转化率
 平衡转化率的是
平衡转化率的是 D.增大
D.增大 浓度
浓度 和一定量
和一定量 的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比(
的混合气体,发生反应Ⅰ,两种气体的平衡转化率(α)与起始的物质的量之比( )的关系如图所示:
)的关系如图所示:
 平衡转化率的曲线为
平衡转化率的曲线为 ”或“
”或“ ”);M点的坐标为
”);M点的坐标为 )水解制备
)水解制备 ,该反应的方程式为:
,该反应的方程式为: 的焓变(
的焓变( )和活化能
)和活化能 ,则合成氨反应
,则合成氨反应 的活化能
的活化能
 。
。 中各组分的“
中各组分的“ ”图像如图:
”图像如图:
 ,逆反应速率为
,逆反应速率为 ,其中
,其中 ,
, 为速率常数,若
为速率常数,若 ,
, ,则A点时刻逆反应速率的计算式为
,则A点时刻逆反应速率的计算式为
 ,平衡常数K=
,平衡常数K= (g)和0.20mol
(g)和0.20mol (g)在恒容密闭容器中发生反应:
(g)在恒容密闭容器中发生反应:

 的转化率为
的转化率为




 (填“大于”“等于”或“小于”)。
(填“大于”“等于”或“小于”)。 的反应体系,标准平衡常数
的反应体系,标准平衡常数 ,其中
,其中 为标准压强
为标准压强 ,
, 、
、 和
和 为各组分的平衡分压,如:
为各组分的平衡分压,如: ,
, 为平衡总压,
为平衡总压, 为平衡系统中NO的物质的量分数。若NO的起始物质的量为1mol,假设反应在恒定温度和标准压强下进行,NO的平衡转化率为
为平衡系统中NO的物质的量分数。若NO的起始物质的量为1mol,假设反应在恒定温度和标准压强下进行,NO的平衡转化率为 ,则
,则
 的最简式表示)。
的最简式表示)。  +
+



 +
+
 H2O+
H2O+

 )、辉铜矿(
)、辉铜矿( )、铜矿(
)、铜矿( )和孔雀石(
)和孔雀石( )。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下:
)。尽管地壳中铁的丰度高于铜,但人类发展炼铁技术的时间较晚。有关铜及其化合物转化的部分工业流程(或转化关系)如下:
 (黑色)、
(黑色)、 (红棕色)、碱式硫酸铜(蓝绿色,如
(红棕色)、碱式硫酸铜(蓝绿色,如 、
、 )等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成
)等。生锈使青铜器的表面呈现出最显著的特征。这一层通常不会改变青铜器的形状,而且铜绿的性质相对稳定,因此通常不会损坏青铜器。然而,如果青铜与含氯物质接触,则可能会形成 和
和 ,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”:
,这被称为“粉末锈病”,这种铜锈会通过以下反应引起“青铜病”: 与
与 和
和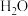 反应,产生
反应,产生 和
和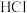 (反应3)。形成的
(反应3)。形成的 不是致密相,进而
不是致密相,进而 穿透松散相,与
穿透松散相,与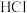 结合并侵蚀
结合并侵蚀 ,从而形成
,从而形成 和
和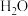 (反应2)。这些反应反复发生,直到器皿完全损坏。
(反应2)。这些反应反复发生,直到器皿完全损坏。 合金)中制备胆矾(
合金)中制备胆矾( )。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加
)。称取一定量的青铜废料,放入烧杯中,在通风橱中小心地向烧杯中加入浓硝酸。在反应过程中,释放出红棕色气体(B),形成蓝绿色溶液(C)与白色沉淀(D)的混合物。过滤后,向滤液中添加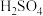 水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。
水溶液,然后形成蓝色溶液E和白色沉淀F。浓缩溶液E和蓝色微晶(晶粒),冷却溶液可获得粗产物(G)。 所有元素化合价都发生了改变,写出固体A的化学式
所有元素化合价都发生了改变,写出固体A的化学式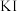 ,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1
,摇晃10秒后,将混合物在黑暗中保持10分钟。加水稀释后,用0.05036mol·L-1 标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数)
标准溶液滴定,滴定终点时消耗20.80mL标准溶液,求出产物的纯度(质量分数)  进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式
进行了热重分析,其重量随温度的变化如下图所示,求出过程中先后得到的三种固体的化学式
 和白色物质X,下列说法正确的是
和白色物质X,下列说法正确的是
A.白色物质X为 ,体现了浓硫酸具有吸水性 ,体现了浓硫酸具有吸水性 |
| B.NO和Y均为还原产物 |
| C.3mol Cu参与反应,转移了6mol电子 |
| D.若稀硫酸足量,在溶解的环节中至少需要0.8mol的稀硝酸 |